A osteonecrose avascular (NA) é uma doença que leva o osso à morte por algum motivo, seja ele direto ou indireto, que pode ser devido a um fator causal ou a vários fatores, e isso secundariamente causa a destruição daquela parte do osso que foi acometida. Vários sinônimos existem para a NA, como Necrose Asséptica da Cabeça Femoral (NACF), necrose atraumática da cabeça femoral e necrose idiopática. Idiopática em medicina é tudo o que não se sabe a causa. Originalmente foi descrita em 1925. A localização mais comum desse tipo de afecção acontece na cabeça femoral. Em 10% dos casos existe além do acometimento do quadril, do joelho e do ombro e em 3% dos casos mais de 3 sítios anatômicos estão acometidos.
Nos Estados Unidos, cerca de 10% das próteses de quadril realizadas todo ano são por necrose avascular da cabeça femoral (NACF). Incide sobre 0,13% da população americana numa prevalência de 10 a 20.000 casos novos por ano. Ocorre em 4 homens para cada mulher acometida e pode ser bilateral em 50 a 80% dos casos. 5 a 22% dos casos precisam de prótese no quadril assim que diagnosticados. Ocorre geralmente na quarta década da vida, mas o espectro etário varia muito. Como muitos pacientes com NACF são muito jovens, talvez a prótese que será implantada no quadril deste paciente não atenda a expectativa de vida que ele tem, e portanto o estudo e o desenvolvimento de novos materiais e superfícies protéticas é fundamental na busca de resultados bons e duradouros. Isso faz com que a tentativa de preservar a cabeça femoral, mesmo na vigência de NACF o quanto se possa seja fundamental.
Os reumatologistas são geralmente os primeiros profissionais a deparar-se com os pacientes, principalmente aqueles que usam corticoides por longo tempo. Mais tarde explicaremos as teorias sobre a culpa dos medicamentos corticosteroides na NACF.
FATORES DE RISCO E COMO ACONTECE A NA
Existe uma lista de fatores de risco para NA. As mais frequentes são o uso de corticoides (doses de >2g de prednisona ou equivalente durante 2-3 meses aumenta o risco), consumo excessivo de álcool e cigarros. Outras inúmeras causas, diretas e indiretas são fratura do colo femoral, luxação coxo-femoral, gravidez, radiação ou radioterapia, quimioterapia, transplantados, reações de hipersensibilidade, doenças mielo-proliferativas, como Gaucher e leucemia, anemia falciforme, trombofilia ou alterações de coagulação, lúpus eritematoso sistêmico, talassemia, disbarismo, disfunções hepáticas, algumas doenças gastro-intestinais e doença dos caixões. Além disso, fatores genéticos também podem estar envolvidos na ocorrência de NA. Em aproximadamente 15% dos casos devemos considerar a NA como idiopática, ou seja, não se sabe a causa. Na verdade, a NA é causada pela interrupção da circulação sanguínea dentro do osso medular da cabeça femoral, ou seja, algo ocluiu os vasos que nutrem a cabeça femoral. Para ocluir um vaso sanguíneo, imagine um êmbolo. Êmbolo é o nome que se dá a um cilindro que dentro de um tubo tem a capacidade de fazer movimento de vaivém. Imagine uma seringa. O mecanismo que permite que o remédio seja injetado é um êmbolo (Figura 1). Quando um êmbolo de qualquer tamanho que seja vai para a circulação sanguínea, provoca embolia.
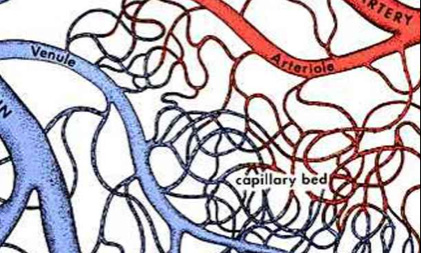
Como a circulação da cabeça do fêmur é terminal, ou seja, a artéria chega até a extremidade do osso e faz uma curva para depois retornar como veia (Figura 2), nesse ponto um êmbolo pode parar e causar a oclusão desse vaso. A oclusão do vaso provoca a morte das células a jusante. Morte da célula é sinônimo de necrose.
Os mecanismos exatos de como ocorre a embolia são desconhecidos. No caso do uso de corticosteroides, o que pode ocorrer é que eles provocam acúmulo de gordura no fígado e essa gordura excessiva pode circular como êmbolos. Nos alcoólatras, uma das consequências do abuso de álcool é a esteatose hepática, num estágio antes da cirrose. Esteatose é sinônimo de gordura acumulada no fígado e gordura, como citado acima, pode circular embolicamente.
As causas diretas, como já foi dito podem ser as fratura do colo do fêmur (pode ocorrer NACF em 16% das fraturas sem desvio e até 30% nas desviadas), as bolhas de nitrogênio nos mergulhadores que não realizam a descompressão adequadamente (doença dos caixões), doenças hematogênicas, que levam a expansão da celularidade da medula óssea, anemia falciforme e fatores que matam diretamente a célula, como radiação ionizante. Radiação ionizante é aquela que se utiliza para radioterapia em tumores, muitas vezes da próstata.
Imagine agora que o pequeno vaso terminal na cabeça do fêmur ocluiu por alguma das causas que citei anteriormente. Todo o osso que estiver depois daquele vaso irá morrer. Todos pensamos que o osso tem cálcio e mais nada, mas no osso temos células ossificadas que são vivas e estão sempre em intenso metabolismo. Quando uma parte desse osso morre, a célula morre mas a matriz mineralizada com cálcio fica. O que fica, apesar de calcificado não tem a resistência mecânica para aguentar a carga que vem de cima. No caso da cabeça do fêmur, o peso vem do lado acetabular. Esse peso acaba por fraturar a cartilagem, que por sinal não é nutrida por sangue (a cartilagem é nutrida pelo líquido sinovial, que é o lubrificante da articulação) e permanece intacta nas primeiras fases da doença. Uma vez fraturada a cartilagem, o processo de deformação do osso morto continua, agora com a entrada de líquido sinovial pela fenda na cartilagem, num ciclo vicioso de dor-deformidade-alteração de função-mais dor.
Fatores genéticos também já foram demostrados. Uma mutação genética no colágeno tipo II, foi achada em 3 famílias, demonstrando herança autossômica dominante. Com relação ao potencial próprio de reparação de lesões, o corpo humano inicia um resposta imediata à morte celular, e em pequenas áreas e localidades da cabeça femoral, pode haver uma resposta satisfatória a ponto de alívio completo dos sintomas. Porém, em mais de 90% dos casos, a resposta orgânica é ineficiente e a doença progride. Com relação aos sintomas, podem aparecer logo após o fator que provocou a NA ou anos após. Geralmente o primeiro sintoma é dor profunda na região da virilha, gradual e que ocasionalmente acontece abruptamente. Pode correlacionar-se com movimentos do quadril e com a carga na articulação quando se caminha, mas em estágios mais avançados pode chegar a doer em repouso. A relação da dor e dos achados nas radiografias não é linear. Pode acontecer de um paciente ter uma grande área de NA com poucos sintomas e vice-versa. Com o decorrer do tempo e com o agravamento das alterações mecânicas provocadas pela deformação progressiva da cabeça femoral, a dor tende a piorar e o arco de mobilidade do quadril diminuir. O tempo em que isso acontece varia de paciente para paciente, de meses a anos. (Figura 3)
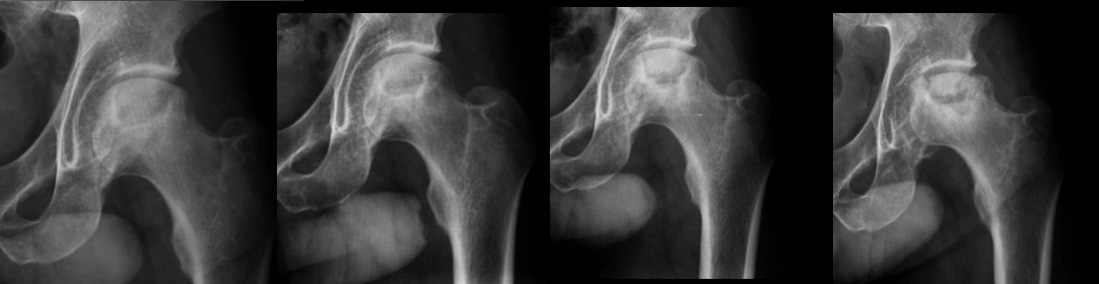
Imagem e progressão radiográfica
Pacientes do grupo de risco ou qualquer um que possua dor profunda na virilha deve ser investigado com exames de imagem. Pesquisa-se também envolvimento de outras articulações ou bilateralidade, que pode acontecer em até 80% dos casos. Além do quadril, outras localizações comuns são joelhos, ombros, tornozelos e cotovelos. A imagem mais apurada para diagnóstico de NA é a ressonância magnética. Outros exames de imagem, como cintilografia, tomografia computadorizada, PET-CT não são necessários para diagnóstico nem para formular plano de tratamento. Pode acontecer de não aparecer nenhuma alteração numa radiografia simples, porém na tomografia e na ressonância magnética a lesão é evidente inclusive demonstrando deformidades (Figura 4).
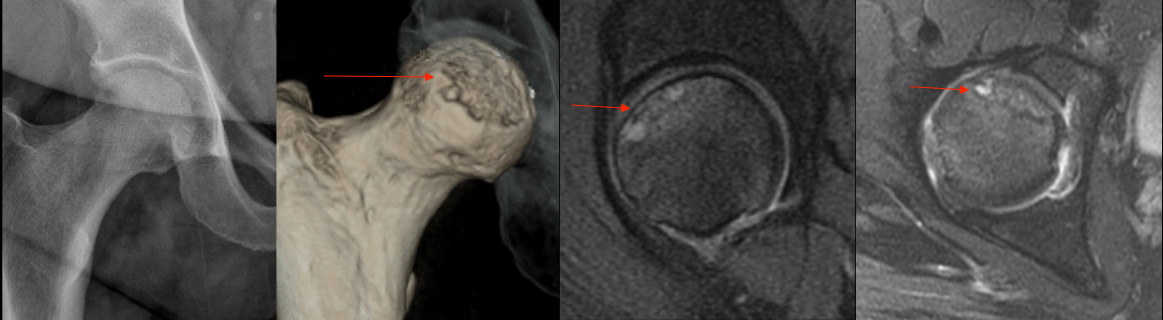
Um grande obstáculo para o estudo da NA é a falta de um método universalmente aceito para classificar a gravidade da doença e assim determinar o prognóstico.
Para se ter uma ideia da falta de padronização, dezesseis diferentes classificações são atualmente utilizadas. Quatro delas, a de Ficat e Arlet, a da Universidade da Pensilvânia , ARCO (Association Research Circulation Osseous) e a da Japanese Orthopedic Association aparecem em mais de 85% de todos os estudos publicados desde 1985. Os estágios de cada classificação estão mostrados na tabela abaixo:
Arlet e Ficat:
I: Normal
II: esclerose óssea ou lesões císticas, sem fratura subcondral
III: Sinal do crescente: há colapso subcondral ou alteração no contorno da cabeça femoral
IV: Artrose com diminuição do espaço articular, osteofitos
Universidade da Pensilvânia:
I,II: os dois primeiros estágios são como a classificação de Arlet e Ficat
III: Sinal da crescente somente
IV: Deformidade no contorno do osso subcondral
V: Diminuição do espaço articular ou alterações acetabulares
VI: Alterações degenerativas avançadas
Cada lesão é dividida em A,B ou C, dependendo da extensão da lesão na ressonância magnética; A: pequena, B: media ou C: grande
ARCO
0: Normal
1: Radiografia e tomografia normais, qualquer outro exame de imagem positivo
2. Esclerose, osteólise, porose focal
3. Sinal do crescente ou achatamento da superfície articular
4. Artrose, comprometimento acetabular ou destruição articular
Comitê Japonês de Investigação:
1. Linha de demarcação, subdividida por área de carga, de medial para lateral, 1A, 1B, 1C
2. Colapso pequeno sem linha de demarcação em torno da área necrótica
3. Lesões císticas, subdivididas pelo local na cabeça femoral, 3ª, medial e 3B, lateral
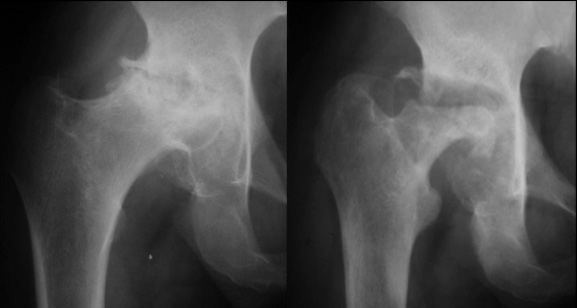
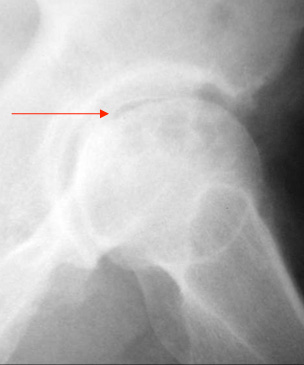
Os parâmetros mais comumente encontrados para mais facilmente padronizar foram com relação a cabeça femoral, as lesões devem ser classificadas em pré ou pós colapso. Casos pré colapso não demonstram o sinal do crescente nas radiografias (Figura 6). As lesões pré colapso têm melhor prognóstico. O tamanho da lesão deve ser medido. Lesões pequenas têm melhor prognóstico. O quanto a cabeça femoral deformou, se for o caso, deve ser medido. Depressões menores que 2 mm. têm melhor prognóstico. O envolvimento do acetábulo deve ser investigado. Quaisquer sinais de artrose tornam o prognóstico pior. A presença ou ausência do sinal da crescente na radiografia, principalmente a tomada com o raio entrando numa inclinação céfalo-caudal de 30 graus, indica o colapso da cabeça femoral como já mencionado e deve ser notada. A presença de esclerose óssea e cistos ao redor da NA deve também ser notada e interfere no prognóstico, para pior caso apareça. Em casos mais graves, o fragmento necrótico e a cabeça femoral podem ser absorvidas, gerando grandes deformidades e encurtamento. (Figura 5). Mais comumente, a área de necrose vai colapsando progressivamente até que a incongruência articular leva a atroes.
Tratamento
1. Tratamento conservador:
A osteonecrose em estágios iniciais pode ser tratada conservadoramente, mas os estágios da doença em que intervenções específicas estão indicadas ainda está para ser estabelecido. Historicamente, a modalidade mais comum de tratamento conservador é tirar a carga da cabeça femoral afetada com bengala ou muletas. A razão para isso é que a carga reduzida irá provocar menor solicitação mecânica na cabeça femoral e na cartilagem e consequentemente retardará sua progressão. Mais de 80% dos casos em que o tratamento conservador foi administrado evoluíram para colapso da cabeça femoral após 4 anos de seguimento.
Em resposta ao mau prognóstico das intervenções não-operatórias, várias outras estão em estudo. A mais comum delas é por meios farmacológicos, oxigenoterapia hiperbárica, terapia de onda de choque e várias modalidades de eletrochoque, como corrente direta e terapia de campo eletromagnético pulsado. O requerimento básico para todas essas opções de tratamento é que eles sejam administrados antes do colapso da cabeça femoral, ou seja, antes que apareça o sinal da crescente nas radiografias. (Figuras 6, 6a e 6b).
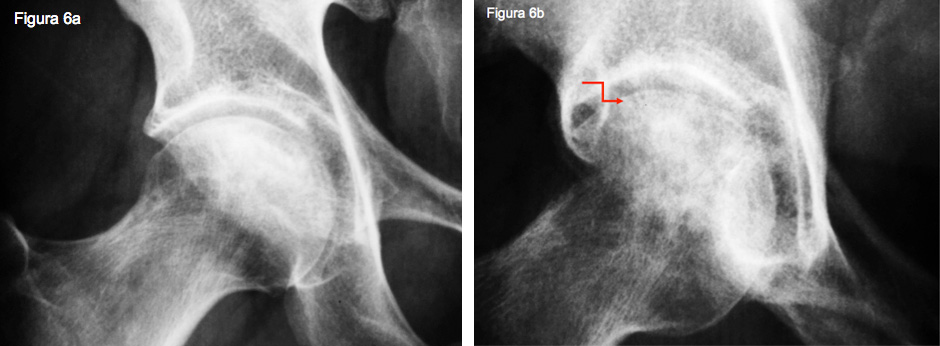
Também há que se salientar que as radiografias sejam tomadas tanto na posição de frente como em perfil e também numa posição de frente com o raio entrando a 30 graus na direção crânio-caudal para podermos visibilizar o sinal da crescente. Interessante observar o que acontece na cabeça femoral quando ocorre a fratura subcondral. Como já dissemos, nas radiografias aparece o sinal da crescente. Na cabeça femoral, aparece também o traço de fratura e, como o osso abaixo está necrótico, toda a matriz viva dentro do osso é reabsorvida, ficando somente o cálcio, deixando logo abaixo da cartilagem um osso duro e desvascularizado. Conforme o tempo vai passando, a resistência mecânica desse osso duro, quebradiço e frágil provoca o afundamento progressivo da cartilagem e deformidades na cabeça femoral. (Figuras 7 e 8)
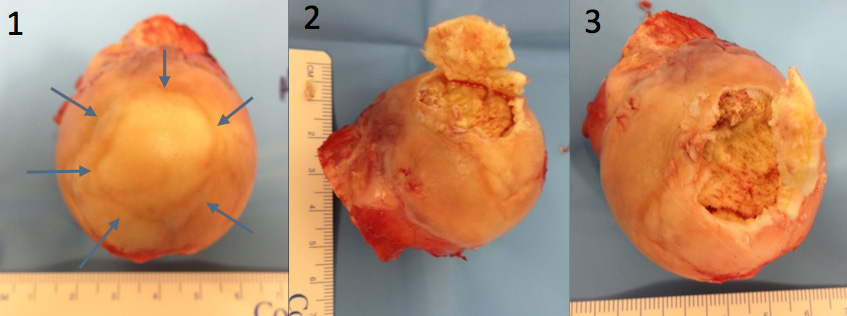
7.2 e 7.3. a área de cartilagem fraturada é frágil: quando se levanta a cartilagem aparece a área de osso necrosado logo abaixo
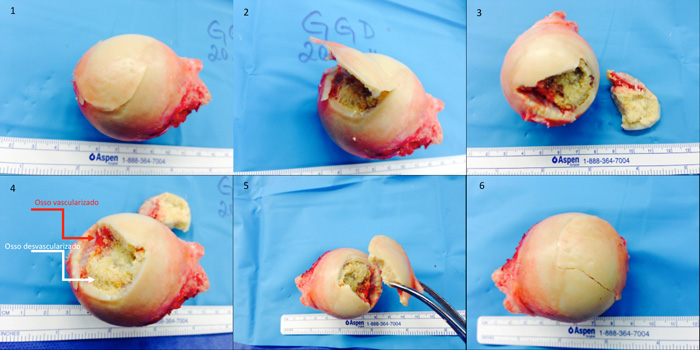
Esse osso já não tem mais vascularização, por isso é esbranquecido. 8.4: Grande área esbranquecida, que contrasta com a área vascularizada atrás, mais vermelha,
onde ainda há circulação. 8.5: Mesmo aspecto, notando-se a cartilagem fraturada, que na figura 8.6, encaixa-se perfeitamente no contorno da cabeça femoral.
Os meios farmacológicos servem para melhorar um ou mais patomecanismos enquanto se permite a revascularização e crescimento ósseo. As drogas mais comuns são vasodilatadores, agentes que baixam os lipídios em circulação, anticoagulantes e bisfosfonados. Vários estudos citam veementemente que novos estudos são necessários para comprovar a verdadeira eficácia dessas drogas. O conceito da câmara hiperbárica é baseado na ideia que a oxigenação aumentada em volta da necrose pode prevenir necrose de áreas ainda maiores e ainda promover a restauração de algum osso em volta. A terapia eletromagnética pulsada, estimulação elétrica direta e terapia de ondas de choque têm a intenção de promover o estímulo à atividade osteoblástica (isto é, formação de osso) e levar ao crescimento de novo osso, o que na teoria fortaleceria o osso em volta e preveniria o colapso. Dentre essas modalidades, apenas a terapia de onda de choque parece surtir algum efeito. Os estudos sobre as outras terapias de choque, direta ou pulsada têm grande ceticismo entre os especialistas.
2. Tratamento cirúrgico:
Muitas opções cirúrgicas são descritas para tratar a NA antes do colapso da cabeça femoral. Alguns cirurgiões utilizam em conjunto com medidas não cirúrgicas descritas acima. Existam 4 modalidades de tratamento cirúrgico para tentar-se preservar ou retardar o colapso na cabeça femoral. Uma delas é a descompressão, outra a osteotomia e enxertos ósseos, que podem ser vascularizados ou não. Podem ainda ser combinados, como a descompressão com uso de enxerto no orifício realizado.
A descompressão parece ajudar em casos de NA em fases iniciais antes do colapso. Alguns autores relatam bons resultados entre 70 e 90% de bons resultados entre 5 e 10 anos de seguimento. O objetivo da descompressão na verdade é aliviar a congestão venosa que causa hiperpressão na cabeça femoral e com isso alivio da dor. Nenhuma técnica de descompressão objetiva fazer reviver o fragmento necrosado ou colapsado. Pode-se também utilizar enxerto ósseo no orifício com o objetivo de dar suporte ósseo a cartilagem que já fraturou e que está sob risco de colapsar. Também se estuda a utilização de terapia de células tronco e mediadores pró-osteogênicos após a descompressão, associado ao enxerto ósseo.
As osteotomias são cortes em algum lugar do fêmur com o objetivo de mudar a posição da área de contato do osso necrótico e tirá-lo do contato direto do acetábulo e da transmissão de força. O procedimento é mais agressivo que a descompressão e seus resultados não reprodutíveis pelos mais diferentes cirurgiões que a utilizam ou que já a utilizaram. Enxertos não vascularizados promovem suporte estrutural ao osso subcondral (logo abaixo da cartilagem) e junto aos enxertos fatores de crescimento ou células tronco podem ser adicionados.
Enxertos vascularizados também podem ser utilizados, mas sua desvantagem é que grandes procedimentos são necessários e uma área doadora, geralmente a fíbula ou a crista ilíaca pode sofrer com a intervenção, cujos resultados também não são reprodutíveis entre diferentes cirurgiões. Nos casos de colapso avançado com artrose e comprometimento funcional, a artroplastia total (prótese) está indicada. Mais de 10% das próteses totais do quadril são feitas por conta da NA.
Mesmo que muitos algoritmos foram propostos para orientar os especialistas no tratamento da NA, a controvérsia permanece sobre qual é o mais apropriado e em qual estágio da doença esses procedimentos devem ser realizados. Em 2005 num esforço para compreender melhor como a comunidade ortopédica da associação americana de cirurgiões de quadril e joelho (AAHKS), fizeram estudo entre os membros associados para determinar a frequência de diferentes procedimentos para tratar a NACF. O mais frequente procedimento na fase pré-colapso foi a descompressão e pós-colapso foi a prótese total do quadril. Interessante resumir um artigo científico, publicado em fevereiro de 2014 por Johnson, et.al. de Baltimore, numa das mais respeitadas publicações ortopédicas do mundo. Estudaram os procedimentos realizados para tratamento da NACF nos Estados Unidos durante 16 anos consecutivos e analisaram quais tendências haviam.
Como resultados, observaram que o número total de procedimentos nesse período aumentou de 3570 para 6400 por ano. Em 1992, 75% dos procedimentos realizados para tratar NA foram prótese total do quadril, que aumentou para 88% em 2008. A percentagem de procedimentos preservadores no quadril consequentemente decresceu de 25 para 12% durante esse mesmo período.
Concluem que antigamente, a prótese total do quadril tinha menor sobrevida e piores resultados clínicos para tratar a NACF, mas os relatos a partir de 1993 sugerem que houve melhora substancial na sobrevida dessas operações e com isso explica-se o aumento substancial na sua indicação e os cirurgiões incorporaram essa modalidade de tratamento na sua prática diária, aumentando o número de próteses realizadas. Ainda mais, o número de procedimentos realizados para NA aumentaram, o que reflete mais conscientização sobre essa doença e também maior possibilidade de diagnosticá-la e trata-la. Uma análise destas é importantíssima, dado que muitos especialistas tratam pequeno número de pacientes e podem não ter uma experiência extensa. Com isso, os autores desse trabalho procuraram conhecer mais sobre a prevalência das opções de tratamento num esforço para entender melhor as tendências ao longo do tempo. As tendências mostradas nesse estudo sugerem que se está utilizando mais prótese de quadril para tratar a NA. Adicionalmente, mesmo que a percentagem de procedimentos de preservação articular diminuíram, o número total de procedimentos, como descompressão e enxertia óssea na área de necrose, aumentou. Isso sugere que, apesar de baixa percentagem, o número de pacientes que recebem um procedimento de preservação e podem nunca ter que receber uma prótese, aumente. (Gráficos 1 e 2).
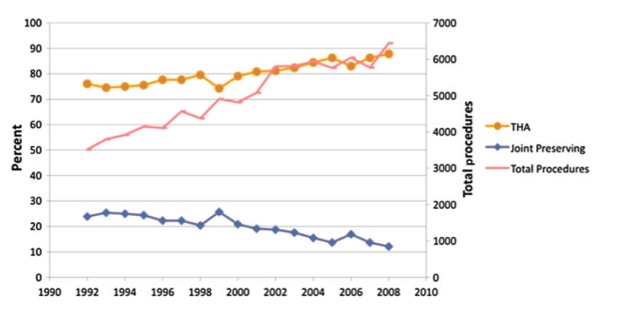
Johnson, et. Al, 2014.
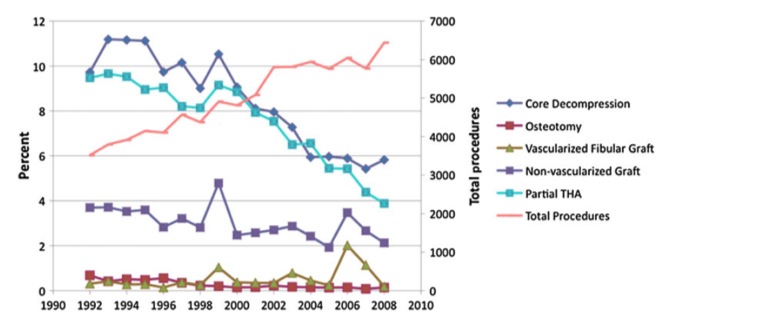
Johnson, et. Al, 2014.
Finaliza frisando que não se recomenda que todos os pacientes que tenham NA sejam tratados com prótese de quadril. Escolhas individualizadas devem ser feitas baseadas na idade, estágio da doença, extensão da área de necrose, experiência do cirurgião e expectativa do paciente. Com esse tema, espero que muitas das suas dúvidas sobre os mecanismos e as possibilidades de tratamento sejam sanadas.
A maior parte desse texto foi baseada no livro: Primer on the Rheumatic diseases, 13th. Ed. Springer Science+Business Media, LLC, 2008. Outras referências úteis para leitura:Johnson, et al.: Treatment of Femoral Head Osteonecrosis in the United States:
16-year Analysis of the Nationwide Inpatient SampleClin Orthop Relat Res (2014) 472:617–623 Banerjee, S. et al: Osteonecrosis of the Hip:
Treatment Options and OutcomesOrthop Clin N Am 44 (2013) 463–476 Haenish,H.Arthritis of the hip(in german) Zentralblatt 1925; 52:1) McGrory, B.J., et al.: Current practices of AAHKS members in the treatment of adult osteonecrosis of the femoral head. J. Bone Jt. Surg. Am 2007: 89: 1194-1204.

